В медной посуде нельзя ни безе взбивать, ни вообще использовать ее там, где она будет контактировать с пищей, питьевой водой и т.п. Медь - это тяжелый металл и является сильным кумулятивным ядом. Микродозы меди, переходящие в раствор из такой посуды, будут поступать в ваш организм и постепенно поражать ваш организм.
Это касается и медных тазов, столь популярных среди любителей дедовских способов варки варенья, и старых плохо облуженных самоваров с блошиного рынка. Разумеется, речь не идет о медной посуде с покрытием - луженой, посеребренной, эмалированной или с покрытием из нержавеющей стали (современная дорогостоящая медная посуда) - в ней медь не контактирует с пищей.
Белок ко всему прочему образует с медью комплекс, значительно повышающий растворимость меди.
Если золото темнеет, значит это не чистое золото, и там содержатся примеси, которые вступая в реакцию окисления дают такой эффект. Чистое золото темнеть не может, но и стоит оно очень дорого, к тому же оно мягкое, примеси в него добавляются, для того, чтобы золотые украшения были прочнее. На примеси может влиять пот человека, в котором содержатся множество веществ, которые могут спровоцировать потемнение, например сера.
Казалось бы, и концентрированная соляная кислота, и концентрированный водный раствор аммиака одинаково хорошо должны дымить на воздухе, потому что оба выделяют газ - хлороводород и аммиак (что легко почувствовать по очень сильному запаху даже на значительном расстоянии от раствора). Однако дымит только соляная кислота. Значит, дело в разных свойствах молекул HCl и NH3. И они в определенном отношении действительно разные. Молекулы хлороводорода в водном растворе диссоциируют практически на 100%, образуя катионы водорода и анионы хлора. Эти ионы в присутствии молекул воды окружают себя огромным количеством этих молекул с образованием многослойной гидратной "шубы" (процесс сопровождается большим выделением тепла). В результате образуются мельчайшие капельки тумана. А молекулы аммиака NH3 не диссоциируют вообще и можно предположить, что молекулы воды к ним "не притягиваются", потому туман не образуется. Кроме того, в водном растворе аммиака ионов NH4+ и ОН- немного, и они гидратируются значительно слабее, чем ионы Н+ и Cl- в растворах соляной кислоты.
В 1827 году 1827 г. датскому химику и фармацевту Вильяму Цейзе понадобилось получить тетрахлороплатинат калия K2[PtCl4]. Эту соль получают из хлорида калия и платинохлористоводородной кислоты H2[PtCl4]. Цейзе знал, что продукт реакции хорошо растворяется в воде и плохо в этиловом спирте. Потому для полноты осаждения продукта он решил провести синтез не в водном растворе, а в спиртом. Однако, прилив к спиртовому раствору кислоты он добавил водный раствор хлорида калия, то вместо ожидаемого красно-коричневого осадка выпал осадок желтого цвета. Его анализ показал, что это не известное ранее вещество, которое имеет необычный состав: KCl∙PtCl2∙C2H4∙H2O, то есть неорганическое соединение содержит молекулу этилена! Было понятно, что этилен получился из спирта, но механизм этой реакции и строение желтого вещества были выяснены только спустя сто лет. Было показано, что образуется комплексная соль, в которой молекула этилена координационно связана с атомов платины. А уравнение реакции такое:
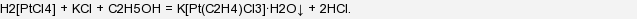
По физическим свойствам гелия можно написать целую книгу, поэтому изложить их здесь, в нескольких строках невозможно. Самый минимум - газ без цвета и без запаха, плотность 178,46 г/м³, температура кипения (сжижения) -268,94°C, температура плавления (затвердевания) -272,2°C.
Химических свойств - НИКАКИХ. Атомы даже не объединяются в молекулы, таак и существуют в виде отдельных атомов. АБСОЛЮТНО НИ С ЧЕМ НЕ РЕАГИРУЕТ.