Вообще-то любая жидкость испаряется при любой температуре окружающей среды. Просто, чем выше температура и ниже насыщенность воздуха парами этой жидкости, тем интенсивнее она испаряется.
При температуре же выше точки кипения этой жидкости она начинает испаряться не только с поверхности, но и по всему объёму. И насыщенность воздуха её парами уже не имеет значения.
Практически каждый школьник знает или хотя бы однажды слышал такое имя, слово, понятие как Авогадро, это не что иное как постоянная величина, она указывает на количество молекул в одном моле вещества, поскольку в вопросе запрашивается количество молекул в 1 моле, то она будет равняться этой постоянной величине:

И это такая цифра - 6,022 Х 10 в 23 степени.
Можно конечно. И естественно приблизительно. Если верить википедии, то масса воды в гидросфере Земле 1,46·10^24 грамм или 8,1·10^22 молей (остальная часть воды (атмосферная, связанная) добавит незначительно) и значит воды на планете Земля 8,1*6,02*10^23*10^22 = 4,9*10^46 молекул.
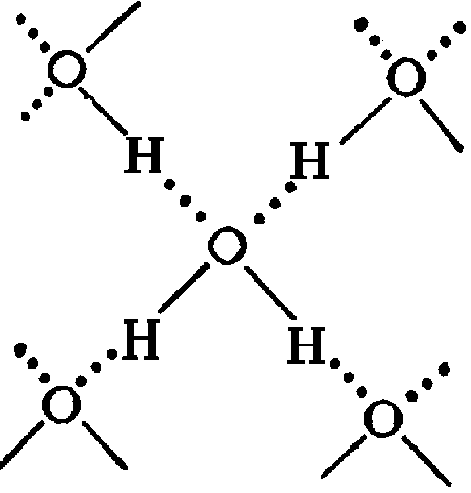
В жидкой воде каждая молекула Н2О, если ее каким-то образом выделить, всегда связана с четырьмя другими молекулами воды, связь осуществляется так называемыми водородными связями. Благодаря этим связям каждый атом кислорода в молекуле Н2О связан с двумя атомами водорода двух соседних молекул Н2О. А каждый атом водорода в молекуле Н2О соответственно связан с одним атомом кислорода "своей" молекулы и одним атомом кислорода соседней молекулы. В результате образуется сплошная сетка связанных друг с другом молекул - примерно как показано на плоском рисунке (в действительности картина объемная). Именно благодаря довольно прочным водородным связям вода имеет аномальные свойства - по сравнению, например, с сероводородом H2S (сера - химический аналог воды, но сероводород становится жидким только при температуре ниже -60°С). Водородные связи легко и очень быстро разрушаются и так же быстро восстанавливаются, но уже в другом порядке. То есть "пунктиры" на рисунке (это водородные связи) и "черточки" (это обычные химические связи) постоянно меняются местами. При этом атомы водорода, принадлежащие одной молекуле, через мгновение принадлежат уже другой молекуле. Время жизни водородной связи составляет примерно от 10^-10 до 10^-11 секунды. Вот такое короткое время и может существовать "данная молекула воды".
Рассчитывать эту цифру следует исходя из химической формулы воды (аш два о) Н2О, у водорода 1 моль будет равен одному грамму, а у кислорода 16 граммов, следовательно, у воды 18 граммов (2 водорода и один кислород) и вода имеет 18 граммов молярной массы на 1 моль.
В одном литре воды 1000 граммов, их разделить на 18 граммов, результат = 55,56 моль, эту цифру умножить на число Авогадро, равное 6, 22 х 10 в 23 степени, перемножив получим:
3,3336 х 10 в 25 степени - количество молекул в 1 литре воды

Конечно, самый простой расчёт всегда для воды, потому что самое знакомое, понятное каждому вещество и не только тем, что более всего используется человеком, ещё потому, что всякий знает её формулу...