Ох уж эта химия... Но мне даже интересно насколько я окажусь права, отвечая на эти, пускай и школьные, задачки.

Cu = 63,546
S = 32,06
масса Cu = (63,546*2)/(63,546*2)+32,06 = 127,1/159,16 = 0,80 или 80%
т.е. в 10 тоннах халькозина масса меди составит 8 тонн.
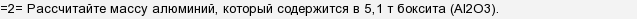
Al = 26,9815
O = 15,9994
масса Al = (26,9815*2)/(26,9815*2+15,9994*3) = 53,97/101,97 = 0,53 или 53%
т.е. в 5,1 тонне боксита масса алюминия составит 2,71 тонны.

C = 12,011
O = 15,9994
N = 14,0067
H = 1,00797
масса N = (14,0067*2)/(12,011+15,9994+(14,0067*2+1,00797*2*2) = 28,02/60,07 = 0,47 или 47%
т.е. в 3 г карбамида содержится 1,41 г азота

Для начала найдёт сколько кальция содержится в одном яйце:
масса Са = 40,08/(40,08+12,011+15,9994*3) = 40,08/100,1 = 0,40 или 40%
Са - 40,08
С - 12,011
О - 15,9994
т.е. с каждым снесенным яйцом организм курицы теряет 4 грамма (10 гр.яйца*40%) кальция. В год курица должна получать не менее 880 (220*10*40%) грамма кальция.

Определим массу хрома в каждой формуле:
масса Cr (1) = (51,996*2)/(55,847+51,996*2+15,9994*2*2) = 104/223,85 = 0,47 или 47%
Fe - 55,847
Cr - 51,996
O - 15,9994
масса Cr (2) = (51,996*2)/(24,305+51,996*2+15,9994*2*2) = 104/192,31 = 0,54 или 54%
Mg - 24,305
Cr - 51,996
O - 15,9994
Итак, в 94 г Fe(CrO2)2 содержится 47% хрома или (94*47%) 44,18 гр, а в 6 г Mg(CrO2)2 содержится 54% хрома (или 6*54%) 3,24 гр. Итого образец хромистого железняка содержит 47,42 грамма хрома.
П.С. ЗА ПРАВИЛЬНОСТЬ РЕШЕНИЯ НЕ ОТВЕЧАЮ, САМОЙ БЫ ХОТЕЛОСЬ УЗНАТЬ НАСКОЛЬКО ВЕРНЫ МОИ ОТВЕТЫ